The Xpert
Xpress CoV-2
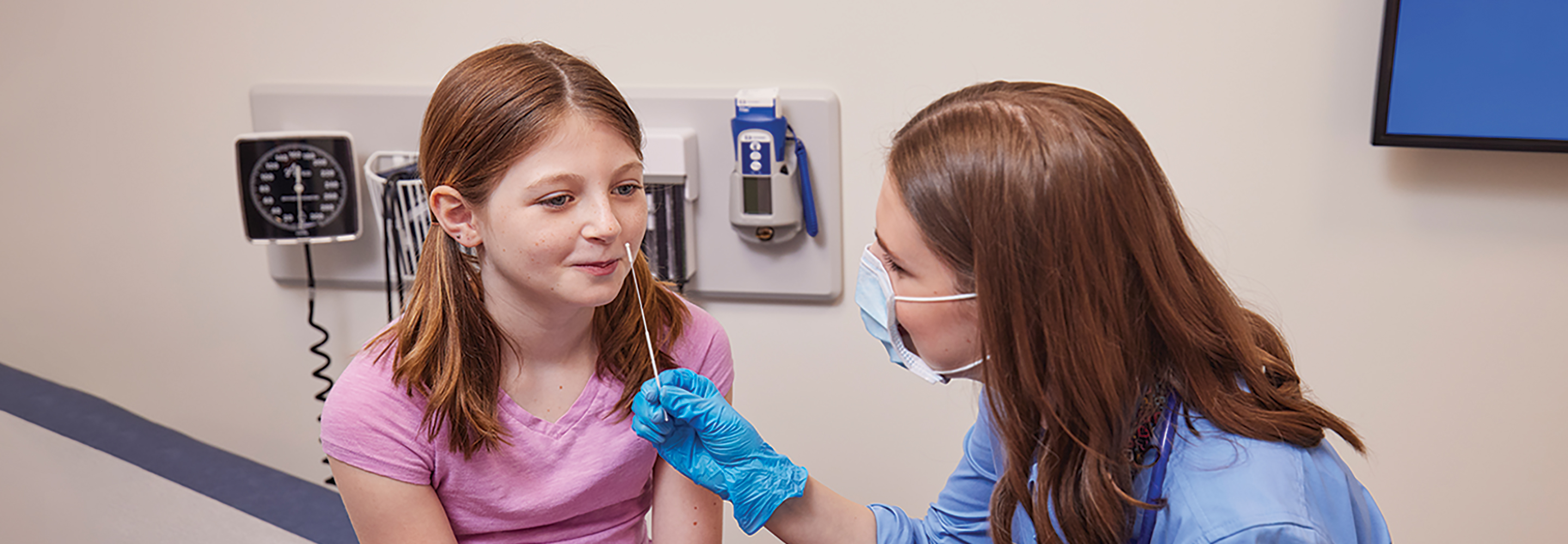
plus test is a rapid, real-time PCR test intended for the qualitative detection of nucleic acid from SARS-CoV-2 in nasopharyngeal swab or anterior nasal swab specimens from individuals suspected of COVID-19 by their healthcare provider, as well as anterior nasal swab specimens from any individual, including from individuals without symptoms or other reasons to suspect COVID-19
The Xpert
Xpress CoV-2
plus test provides:
- Fast and accurate results in as early as 20 minutes*
- Three gene targets for the detection of SARS-CoV-2, providing target redundancy to mitigate potential impact of genetic mutation
- Rapid sample-to-answer testing with actionable results and minimal hands-on-time
* With early assay termination for positives, otherwise, the full test runtime is 30 minutes.
CE-IVD. In-vitro-Diagnostikum. Eventuell nicht in allen Ländern erhältlich.